Un po' di teoria

Introduzione
Questi articoli NON vogliono essere in alcun modo una spiegazione esauriente dell'argomento spettroscopia. Lo scope invece e di gettare le basi per creare una curiosita' nel lettore che lo spinga a effettuare ricerche piu' approfondite e trattazioni complete scritte da chi ha titolo per farlo. In base a questo obbiettivo quanto segue sara' volutamente semplificato per non appesantire l'approccio e favorire invece la comprensione dei principi di base.
Tutti quanti abbiamo visto l'arcobaleno dopo un temporale, almeno credo... Questo fenomeno atmosferico e' un esempio lampante di spettroscopia! La luce del sole attraversa le goccioline d'acqua in sospensione nell'atmosfera e per effetto della dispersione la luce viene separata in tutti i suoi colori. Non e' chiaro? bene... un passo indietro...
La luce e' energia sotto forma di onda elettromagnetica (anche se per la meccanica quantistica e' una particella, ma non e' questa la sede per discutere il dualismo onda-particella della luce...). La luce, come tutte le onde ha una frequenza e il nostro occhio e' sensibile a un insieme di frequenze ben preciso chiamato “Spettro Visibile”. In questo range di frequenze che va da circa 4000A a 7000A l'occhio discerne i colori in base alla frequenza specifica. Cosi' se il nostro occhio viene colpito da luce a 4500A questa ci apparira' blu, a 5000A ci apparira' verde e 6500 ci apparira' rossa.
Dispersione in prisma
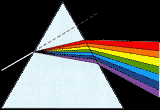
Un raggio di luce bianca e' quindi formato da onde di ogni colore ovvero di ogni frequenza (comprese nello spettro visibile ovviamente).Quando un raggio di luce bianca attraversa un pisma di vetro accade che i raggi di diverse frequenze subiscono una dispersione (deviazione) ad angolo differente. Quindi per esempio il rosso viene deviato piu' del verde che viene deviato piu' del blu. Il risultato e' che all'uscita dal prisma la luce e' stata "scomposta" e si osserva un arcobaleno.
Lo stesso risultato si puo' ottenere invece che per dispersione per diffrazione. In questo caso la luce attraversa un supporto trasparente solcato da numerosissime fessure. Per un effetto ottico chiamato diffrazione la luce si "separa" producendo un arcobaleno.
Esistono griglie che devono essere attraversate dalla luce e griglie che invece riflettono la luce. Queste ultime possono arrivare a 1200 fessure per millimetro. I sistemi per diffrazione sono molto piu' efficenti e permettono di ottenere "arcobaleni" molto piu' dettagliati di quelli ottenuti con i prismi.
Abbiamo visto che e' possibile scomporre la luce nella sue frequenze elettromagnetiche, producendo una striscia colorata simile all'arcobaleno. Questo arcobaleno si chiama “spettro” ed e' una piccola meraviglia della natura dato che in esso e' possibile leggere una incredibile quantita' di informazioni.
Supponiamo che una luce bianca colpisca direttamente e nel vuoto nel vuoto la griglia di diffrazione. In uscita (o ad un certo angolo da essa nel caso di griglie a riflessione) dalla griglia osserveremo uno spettro colorato contenente tutti i colori dal rosso scuro fino al viola acceso, ovvero dai limiti dell'infrarosso a quelli dell'ultravioletto che sono poi i limiti del nostro occhio.
I colori di questo spettro cambieranno uno nell'altro senza soluzione di continuita' e in modo graduale. Questo e' uno spettro teorico che ci dice di quali colori (frequenze) e' composta la luce in arrivo ma niente di piu'.
Supponiamo adesso che la luce bianca prima di colpire la grata di diffrazione attraversi un gas, nella fattispecie Idrogeno (simbolo chimico H). All'uscita della grata osserveremo ugualmente uno spettro colorato ma una analisi attenta rivelera' che su di esso sono improvvisamente comparse delle righe nere. Ovvero in alcuni punti lo spettro sembra interrompersi. Ripetiamo l'esperimento ma facciamo attraversare alla luce del gas Elio (simbolo chimico He) invece che dell'Idrogeno. Anche in questo caso otteniamo uno spettro con delle righe scure ma in posizioni diverse dalle righe scure ottenute dall'attraversamento dell'idrogeno.

Bande di assorbimento dell'idrogeno
Se andiamo avanti con tutta la tavola periodica arriviamo rapidamente alla conclusione che ogni elemento chimico produce quando attraversato dalla luce uno spettro con ben detrminante righe scure, dette bande di assorbimento. Ogni elemento chimico ha una sua firma, che appone alla luce ogni volta che questa lo attraversa. Vi risparmio la spiegazione quantistica (un delizioso giochetto di livelli energetici degli elettroni et similaria...) di questa cosa e ve ne fornisco un'altra meno precisa ma forse piu' semplice. In pratica e' come se ogni elemento fungesse da filtro per certe frequenze di luce. Quando la luce attraversa l'idrogeno o l'elio riesce a passare oltre "quasi" tutta ma non tutta. Quel po' di luce che non passa oltre il materiale e' tutta concentrata in alcune frequenze ben precise. Quando poi si estrae lo spettro ecco che in corrispondenza di questi assorbimenti compaiono le righe nere che indicano assenza di luce per quella frequenza.
Lo stesso fenomeno puo' prodursi in senso opposto. Se una luce con sufficente energia colpisce un gas e lo ionizza, al termine di un certo numero di passaggi il gas emette a sua volta luce, su frequenze ben precise caratterstiche del gas stesso. In questo caso la luce produce uno spettro con righe piu' chiare al posto di quelle piu' scure.

Bande di emissione dell'Idrogeno
La conclusione di questo discorso e' quindi che studiando la luce di una stella, ottenendone lo spettro e analizzando le righe di assorbimento in esso presente e' possibile risalire ai materiali che compongno la stella. La luce infatti viene prodotta nel cuore dell'astro e deve attraversare tutti gli strati superiori per arrivare a noi. Ogni elemento chimico attraversato lascia la sua impronta sulla luce e noi qui possiamo risalire alla composizione chimica.
|